Anatomie & Physiologie: Atmungssystem
Dr. John V. Urbas, <dr.john.urbas@online.de>

Dr. John V. Urbas, <dr.john.urbas@online.de>
Die Kategorien des Atmungsprozesses
Der Atmungsprozess wird von Physiologen in die folgenden drei Kategorien unterteilt:
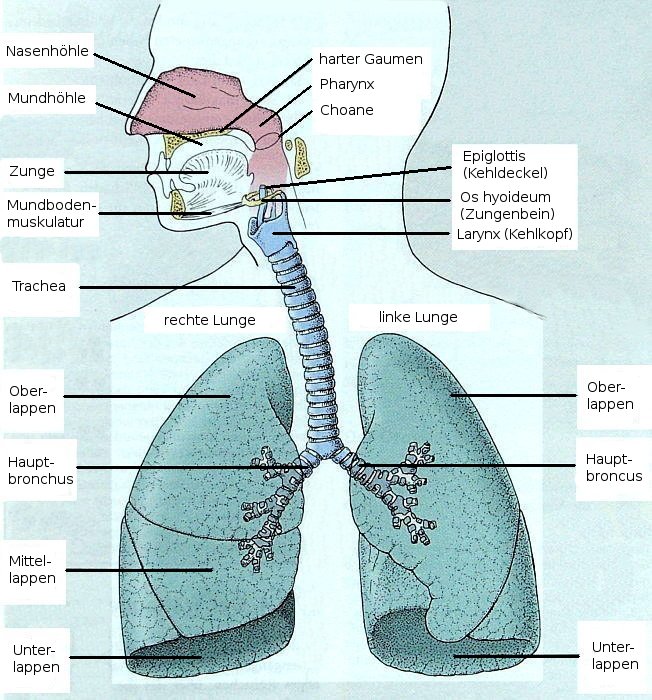
Der obere und der untere Respirationstrakt
Das Atmungssystem wird durch die Epiglottis (den Kehlkopfdeckel) in zwei Teile getrennt:
Nasus externus
Die sichtbaren Teile der äußeren Nase (Nasus externus):
Cavitas nasi (Nasenhöhle)
Die Nasenhöhle ist der wesentlich größere innere Anteil der Nase (Abb. 1).
Septum nasi
Das Septum nasi (Nasenscheidewand) unterteilt die Nasenhöhle in zwei Kammern.
Die Oberfläche der Seitenwände der Nasenhöhle wird durch die Concha nasalis inferior (untere Nasenmuschel), Concha nasalis media (mittlere Nasenmuschel) und Concha nasalis superior (obere Nasenmuschel) vergrößert.
Es gibt drei wesentlichen Funktionen der Nase.
1. Erwärmung, Vorreinigung und Anfeuchtung der Atemluft
Die Nasenhöhle ist von einer Schleimhaut überzogen, an deren Oberfläche sich ein mehrreihiges Flimmerepithel mit Flimmerhärchen (Cilia, Zilien, Abb. 1) befindet.
2. Beherbergung des Riechorgans
Im Dach der Nasenhöhle liegt die Regio olfactoria (das Riechorgan), die sich direkt unter der Lamina cribrosa des Siebbeins befindet.
3. Resonanzraum für die Stimme
Die Resonanz der Stimme wird von der Nasenhöhle und viel mehr von den Nasennebenhöhlen bestimmt.
Der Pharynx (Rachen, Schlund)
Der Pharynx ist eine Art Muskelschlauch, der sich von der Schädelbasis bis zum Ösophagus (Speiseröhre) erstreckt (Abb. 1).
Der Larynx (Kehlkopf)
Der Larynx lässt sich insbesondere beim Mann durch den sog. Adamsapfel an der Vorderseite des Halses leicht abtasten.
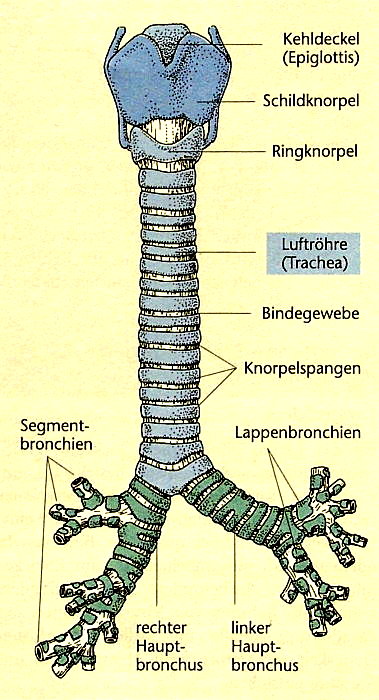 Der Larynx enthält und schützt die Stimmbänder. Seine
Form erhält er durch fünf Knorpelstücke, die durch
Bänder sowie durch an Außen- und Innenseite verlaufende
Muskeln verbunden sind. Die drei größten Stücke sind:
Der Larynx enthält und schützt die Stimmbänder. Seine
Form erhält er durch fünf Knorpelstücke, die durch
Bänder sowie durch an Außen- und Innenseite verlaufende
Muskeln verbunden sind. Die drei größten Stücke sind:
Der gesamte Larynx, mit Ausnahme der Epiglottis und der Stimmbänder, ist von einer gefäßreichen Schleimhaut ähnlich der Nasenschleimhaut bedeckt.
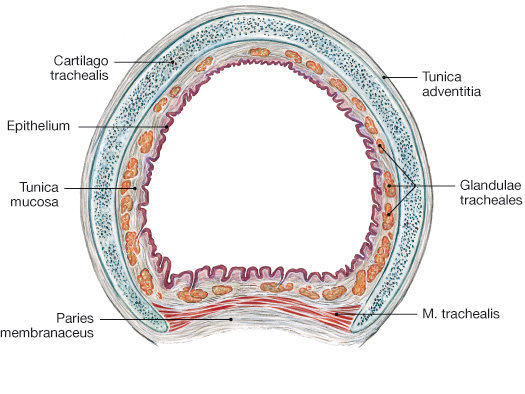
Trachea (Luftröhre)
Unterhalb des Ringknorpels beginnt die etwa 11 cm lange Trachea (Luftröhre). Sie endet an der Bifurcatio tracheae, wo die beiden Hauptbronchien (Bronchus principalis dexter und Bronchus principalis sinister) entstehen (Abb. 1).
Übersicht
Unter funktionellen Gesichtspunkten unterscheidet man zwei Abschnitte des Bronchialbaums:
Der konduktive Abschnitt
Dieser Teil führt dem respiratorischen Abschnitt Atemluft zu bzw. transportiert sie wieder ab, ohne dass er selbst am Gasaustausch mit dem Blut beteiligt ist.
Nach wenigen Zentimetern teilen sich die Hauptbronchien in kleinere Bronchien.
Schon auf der Ebene der Lappenbronchien werden die Knorpelspangen durch unregelmäßige Knorpelplättchen ersetzt.
Der respiratorische Abschnitt
Dieser Abschnitt ist verantwortlich für die Sauerstoffaufnahme aus der eingeatmeten Luft in das Blut des Kapillarsystems der Lungebläschen.
Die Bronchiolen verzweigen sich in mikroskopisch feine Ästchen, die man Bronchioli respiratorii nennt.
Bei körperlicher Ruhe ist ein erheblicher Teil der Alveolen nicht belüftet.
Die zarte Struktur der Alveolen wird durch einen monomolekularen Flüssigkeitsfilm (den sog. Surfactant) geschützt.
Wegen des Surfactants und der Zahl der elastischen Fasern im Lungengewebe hat die Lunge ihre wichtige Eigenelastizität, die sogenannte Compliance.
Übersicht
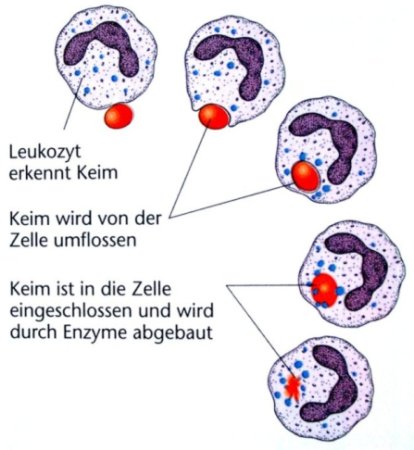
Die Lunge verfügt über drei Reinigungsmechanismen:
Tracheobronchiale mukoziliäre Clearance
Die tracheobronchiale mukoziliäre Clearance wird auch als mukoziliäres Transportsystem bezeichnet.
Funktion
Der Hustenmechanismus ist auch ein sehr wichtiger Schutzfaktor für die Atemwege.
Der Hustenvorgang läuft in fünf Phasen ab.
Die folgenden vier Phasen sind:
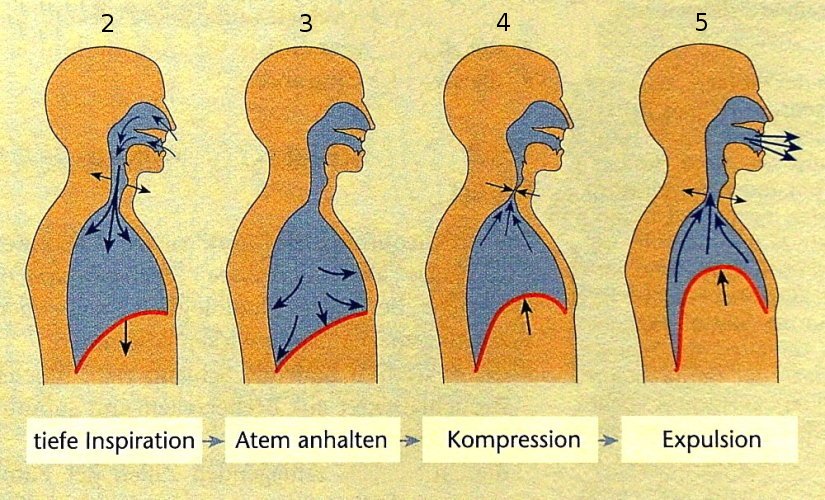
Säuberung der Lungenbläschen
Ab der 7. Bronchiengeneration ist die Husten-Clearance nicht mehr effektiv. Ab etwa der 16. Bronchiengeneration gibt es keine mukoziliäre Clearance.
Lage
Struktur
Die Hauptbronchien, Nerven und die Lungengefäße treten über den an der medialen Seite einer jeden Lunge gelegenen Lungenhilus (Hilum pulmonis, Lungenwurzel) in die Lungen ein. Der Lungenhilus bildet den Zugang für:
Gleichzeitig ist das Hilum pulmonalis die Ausgangsstelle für:
Übersicht
Die Gliederung des Lungengewebes in Lappen, Segmente, Läppchen und Azini liegt jeweils eine Struktur des Bronchialbaums mit seinen weiteren Verzweigungen zugrunde (Tab. 1).
Lungenlappen
Die linke Seite des Bronchialbaums hat zwei Lappenbronchien. Entsprechend hat die linke Lunge zwei Lungenlappen: einen Oberlappen und einen Unterlappen.
Die rechte Seite des Bronchialbaums hat drei Lappenbronchien. Entsprechend hat die rechte Lunge drei Lungenlappen: einen Oberlappen, einen Mittellappen und einen Unterlappen.
Die Unterlappen liegen vorwiegend der hinteren Brustwand an, die Oberlappen und der rechte Mittellappen liegen dagegen vorwiegend vorne.
Lungensegmente
Die Lungensegmente sind wichtige funktionelle Einheiten der Lunge.
Lungenläppchen (Lobulus)
Ein Lungenläppchen besteht aus 5 bis 12 Lungenazini, ist aber makroskopisch meist schlecht abzugrenzen.
Lungenazinus
Als Lungenazinus bezeichnet man die funktionelle Einheit von Bronchiolus terminalis, dem anschließenden Gangsystem und den zugehörigen Alveolen.
Die Lungennerven
Beide Teile (der Sympathikus und der Parasympathikus) des vegetativen (autonomen) Nervensystems versorgen die Lungen.
Pleurablätter
Die hauchdünne Pleura visceralis (= Lungenfell) überzieht beide Lungen. Diese mit Gefäßen versorgte Lungenhülle grenzt, nur durch einen flüssigkeitsgefüllten Spalt getrennt, an die Pleura parietalis (= Rippenfell).
Im Pleuraspalt herrscht immer ein Unterdruck (der sog. intrapleurale Druck) zwischen 5 mmHg unter dem äußeren Luftdruck (d.h. -5 mmHg) am Ende der Inspiration (Einatmung) und -3 mmHg am Ende der Exspiration (Ausatmung).
Definition und Folgen
Als Folge einer Stichverletzung oder des Platzens von Alveolen kann Luft in den Pleuraspalt gelangen. Es ensteht ein Pneumothorax.
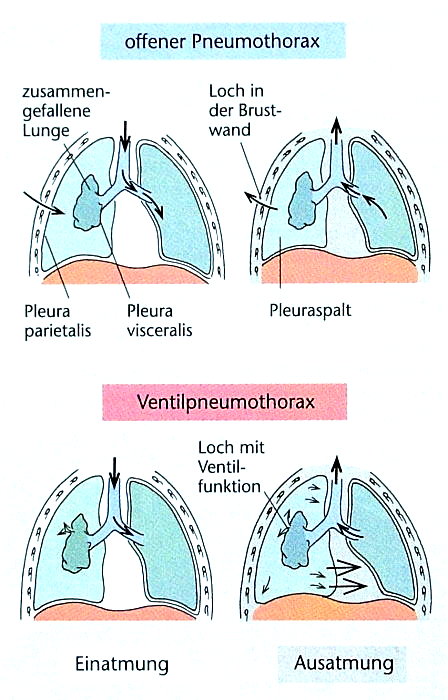
Ventilpneumothorax (Spannungspneumothorax)
Der Ventilpneumothorax ist eine akut lebensbedrohende Notfallsituation!
Eine rasche Entfernung der Luft aus dem Pleuraspalt durch eine geeignete Vakuumpumpe (Pleuradrainage) kann hier das Leben retten.
Definition, Entstehung und Formen
Unterschiedliche Krankheitsprozesse können zu einer Ansammlung von Flüssigkeit im Pleuraspalt (= Pleuraerguss) führen:
Entzündungs- oder tumorbedingte Ergüsse beruhen auf Veränderungen in der Durchlässigkeit der Kapillaren.
Ein Erguss als Folge einer linken Herzinsuffizienz ist durch einen erhöhten Gefäßdruck bedingt.
Wird das Ergussvolumen groß (mehrere Liter) kann der Pleuraspalt so weit ausgedehnt werden, dass eine ausreichende Entfaltung der Lunge nicht mehr möglich ist und Atemnot auftritt.
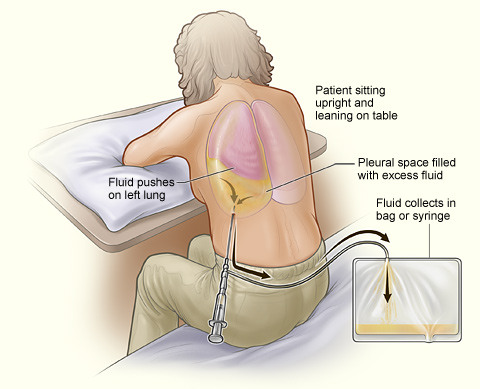 Hier kann eine Pleurapunktion (auch
Thoracentesis oder Thoracocentesis genannt) Abhilfe
verschaffen: Eine Punktionsnadel wird in den Pleuraspalt
eingeführt und das Sekret wird abgesaugt
(= Pleuradrainage)
Hier kann eine Pleurapunktion (auch
Thoracentesis oder Thoracocentesis genannt) Abhilfe
verschaffen: Eine Punktionsnadel wird in den Pleuraspalt
eingeführt und das Sekret wird abgesaugt
(= Pleuradrainage)
Atemzug
Ein Atemzug umfasst zwei Phasen:
Da die Lunge elastisch aber selbst nicht beweglich ist, folgt sie bei den Atembewegungen die Erweiterung und Verengung des Brustkorbs.
Atemfrequenz
In Ruhe hat ein Erwachsener 12–16 Atemzüge/Min (die Atemfrequenz), ein Kind aber bis zu 25 Atemzüge/Min. Die Atemfrequenz ist also stark altersabhängig.
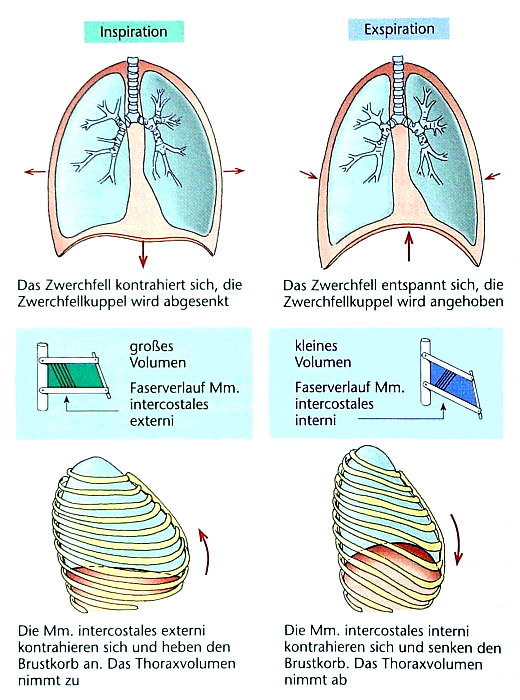
Die Inspiration
Die Inspiration erfolgt durch die Kontraktion des Diaphragma. Bei vertiefter physiologischer Inspiration übernimmt es zwei Drittel der Erweiterungsarbeit des Brustkorbinnenraumes.
Die Atemhilfsmuskulatur
Bei vertiefter Atmung, z.B. bei Atemnot, wird die Inspiration durch sog. Atemhilfsmuskeln unterstützt. Um diese Wirkung zu entfalten, müssen die meisten Atemhilfsmuskeln bei fixiertem Ansatz kontrahiert werden.
Damit die Atemhilfsmuskeln optimal arbeiten können, muss eine besondere atemerleichternde Körperstellung eingenommen werden.
Die Exspiration
Die Exspiration geschieht überwiegend passiv.
Die Atemhilfsmuskulatur
Die Exspiration wird zu 95% von dem Diaphragma kontrolliert. Zur Unterstüzung der Exspiration kann man die folgenden Muskeln auch aktivieren:
Übersicht
Abhängig von Körpergröße und Körperbau treten bei jedem Atemzug etwa 500 ml Luft in den Respirationstrakt ein.
Bei einigen Krankheiten kann der anatomische Totraum dramatisch zunehmen, wie beim Lungenemphysem mit einer großen Anzahl von zerstörten Alveolen.
Neben dem anatomischen Totraum gibt es auch einen sog. alveolaren Totraum (auch funktionellen Totraum genannt).
Einführung
Bei vielen Erkrankungen von Herz und Lungen sind genaue Kenntnisse über die ein- und ausatembaren Luftvolumina und deren Flussgeschwindigkeit in den Atemwegen wichtig.
Die Werte variieren von Person zu Person stark.
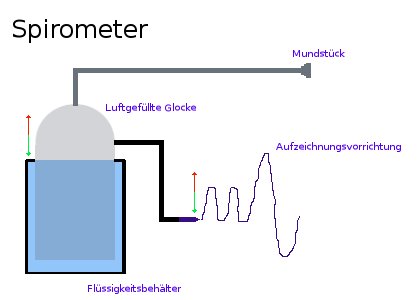
Spirometrie
Die Messung der mobilisierbaren Lungenvolumina erfolgt mit Hilfe eines Spirometers und wird deshalb Spirometrie genannt.
|
|
Im Alter nimmt die Vitalkapazität schneller als die Totalkapazität ab.
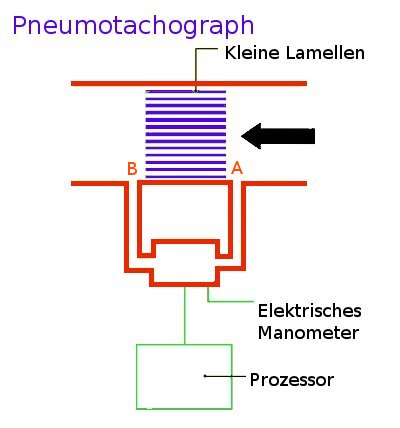
Der Tiffeneau-Test
Beim Tiffeneau-Test (auch Einsekundenkapazität genannt) muss der Patient nach vorheriger maximaler Einatmung so schnell und so tief wie möglich in ein Spirometer ausatmen.
Eine Verengung der Atemwege kann verschiedene Ursachen haben:
Einführung
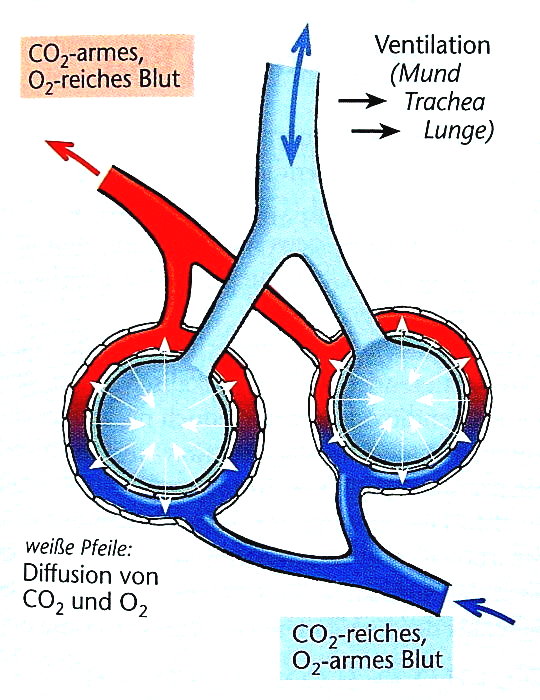
Unter dem Begriff Ventilation verstehen wir die Belüftung der Lunge.
Die ausreichende Ventilation der Lunge ist eine entscheidende Voraussetzung für den Gasaustausch in den Alveolen: ohne Belüftung der Alveolen kann kein O2 in die Blutbahn aufgenommen oder CO2 in die Atemluft abgegeben werden.
Die Lage
 Die gesamte innere Oberfläche der Alveolen (die
Gasaustauschfläche) beträgt beim Erwachsenen etwa 100
m2.
Die gesamte innere Oberfläche der Alveolen (die
Gasaustauschfläche) beträgt beim Erwachsenen etwa 100
m2.
Die O2- und CO2-Moleküle diffundieren dazu durch die maximal 1 µm dicke sog. Blut-Luft-Schranke:
Wie in Abb. 1 zu sehen, ist der O2-Gehalt der Einatemluft ca. 20%.
Ventilation und Perfusion
Ein effizienter Gasaustausch verlangt eine gute Abstimmung der Perfusion (Durchblutung) auf die Ventilation der Alveolen.
Der Euler-Liljestrand-Reflex
Der Euler-Liljestrand-Reflex verursacht beim O2-Mangel in einem bestimmten Lungenanteil, dass die dazugehörigen Kapillaren sich verengen — die eingeschränkte Belüftung eines Lungenabschnittes (= O2-Mangel) sorgt dafür, dass das Blut in die gesunden Lungenanteile strömt (durch Verengung der Kapillaren im eingeschränkt belüfteten Lungenabschnitt).
Störungen
Ist der Austauschweg zwischen Alveolen und Kapillarinnenraum länger als normal (= dickere Blut-Luft-Schranke, wie z.B. bei einer Lungenfibrose mit vermehrter Bindegewebsbildung zwischen den Alveolen), kann es zu einer Dyspnoe (Atemnot) kommen.
Fällt der O2-Gehalt des Blutes unter den Normalwert ab, so spricht man von Hypoxämie.
Sauerstofftransport
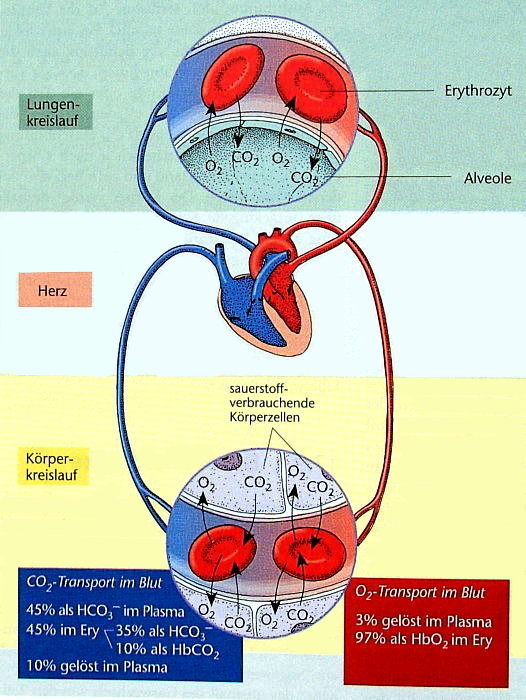 Der Sauerstoff wird über die Lunge ins Blut aufgenommen.
Der Sauerstoff wird über die Lunge ins Blut aufgenommen.
Der aufgenommene Sauerstoff wird in zwei Formen transportiert:
Normalerweise findet man ca. 15 g Hb in 100 ml Blut eines gesunden Erwachsenen.
Die O2-Kapazität des Blutes, d.h. die O2-Menge, die im Blut transportiert werden kann, wird durch Hb um das 70-fache erhöht.
In den Kapillarnetzen des systemischen Kreislaufes wird O2 ans Gewebe abgegeben.
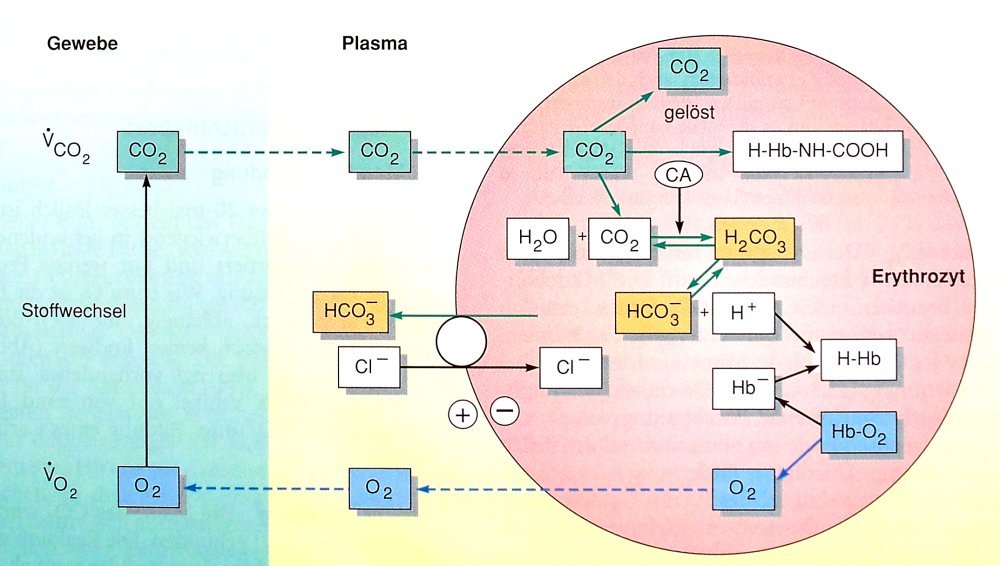
Kohlendioxidtransport
Das Kohlendioxid wird über die Gewebekapillaren ins Blut aufgenommen.
Einführung
Lungenerkrankungen verursachen häufig ein Ungleichgewicht zwischen Ventilation (Belüftung) und Perfusion (Durchblutung) der alveolaren Bereiche der Lunge.
Restriktive Ventilationsstörungen
Hier haben die Betroffenen eine eingeschränkte Ausdehnungsfähigkeit von Lunge und Thorax.
Restriktive Ventilationsstörungen haben verschiedene Ursachen, z.B.:
Die Physiotherapie spielt eine bedeutende Rolle für Patienten mit restriktiven Ventilationsstörungen.
Obstruktive Ventilationsstörungen
Bei diesen Störungen werden die Strömungswiderstände in den Atemwegen erhöht. Die Vitalkapazität bleibt normal, aber die Ausatmung ist erschwert und die Atemwege können kollabieren (Bronchialkollaps). Einige Beispiele sind:
Übersicht
Störungen in der Durchblutung der Lunge beeinträchtigen sowohl die Atmungs- als auch die Kreislauffunktion. Sie bedrohen daher im besonderen Maß das Leben des Patienten. Beispiele der wichtigsten Perfusionsstörungen sind:
Atemzentren des Hirnstamms
Das Steuersystem für die Atmung liegt in der Medulla oblongata (dem verlängerten Mark) des Hirnstamms.
Die rhythmische Aktivität der Atemzentren kann über zahlreiche Faktoren modifiziert werden.
Zentrale und periphere Einflüsse
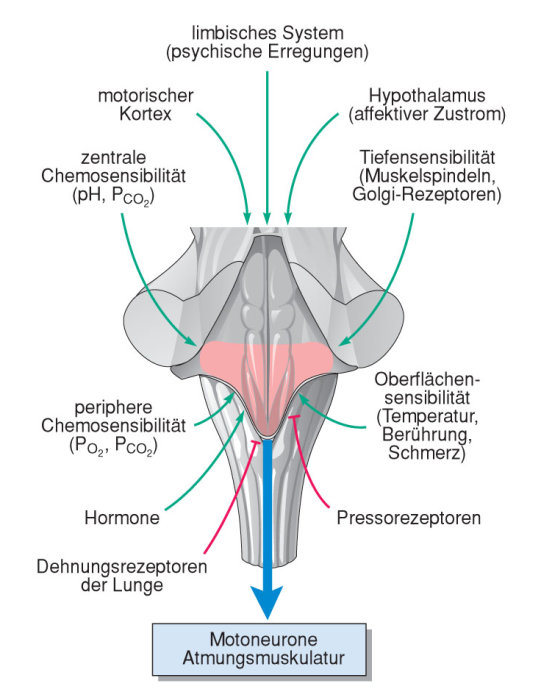 Weitere afferente und efferente Einflüsse kommen über die
verschiedensten Wege in die Atemzentren an
Weitere afferente und efferente Einflüsse kommen über die
verschiedensten Wege in die Atemzentren an
Chemische Kontrolle der Atmung
Die drei arteriellen Werte von pH, PO2 und PCO2 können bei Abweichungen von ihrem Normalwert über spezifische Chemorezeptoren die Ventilation so beeinflussen, dass der für die Stoffwechselprozesse optimale Zustand wiederhergestellt wird. Die Atemtätigkeit wird erhöht durch
Die peripheren Chemorezeptoren
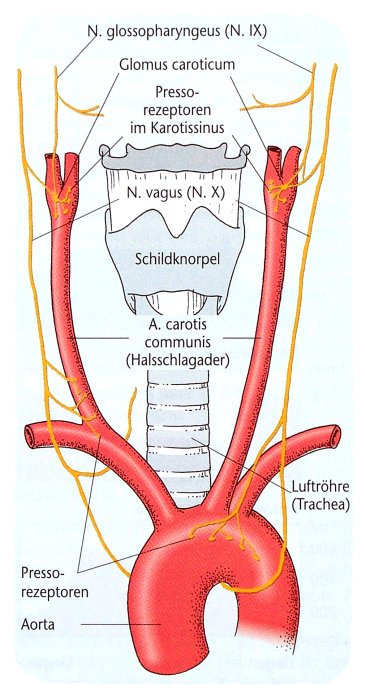 Die drei obengenannten Regelgrößen werden über
Chemorezeptoren im Glomus caroticum sowie im
Aortenbogen gemessen.
Die drei obengenannten Regelgrößen werden über
Chemorezeptoren im Glomus caroticum sowie im
Aortenbogen gemessen.
Die zentralen Chemorezeptoren
Die sog. zentralen Chemorezeptoren befinden sich an der ventralen Oberfläche der Medulla oblongata (Abb. 1) in der Nähe der respiratorischen Neuronen
Klinik
Bei Patienten mit chronischen Atemwegserkrankungen finden sich ständig erhöhte CO2-Konzentrationen im Blut (chronische Hyperkapnie).
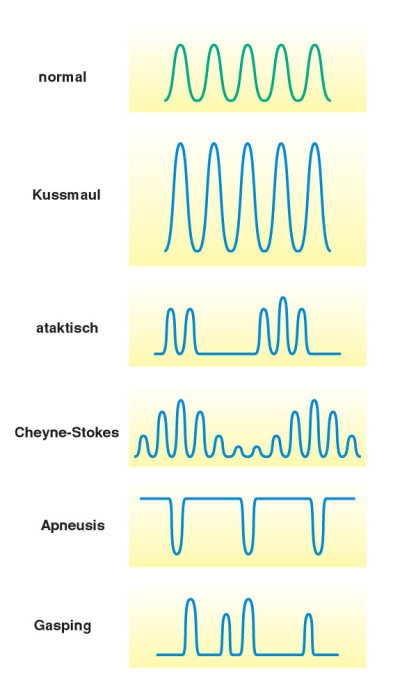
Überblick
Bei vielen Lungen- und Kreislauferkrankungen kommt es zu einem Anstieg des arteriellen PCO2. Dieser Zustand der CO2-Überladung wird als Hyperkapnie bezeichnet. Bei einer Hyperkapnie treten krankhafte Atmungsformen auf.